
- Overview
-
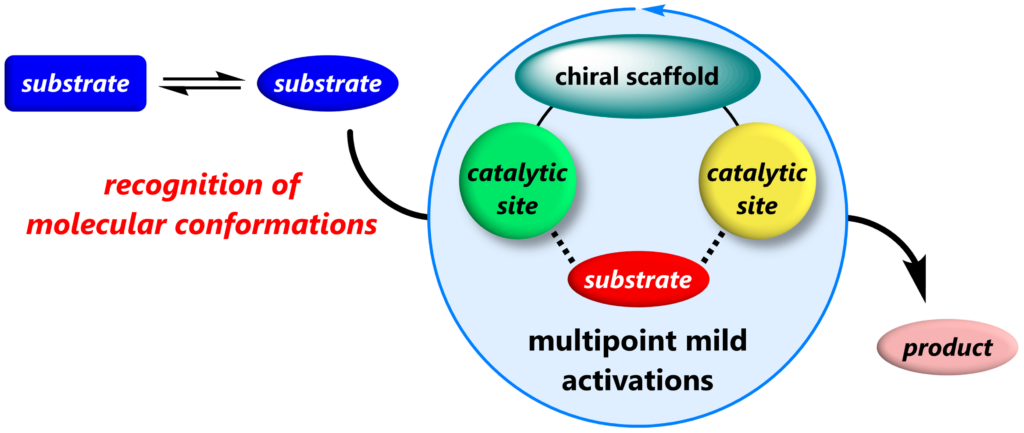
有機触媒は様々な分子間相互作用を利用して基質分子を活性化します。その強度は金属触媒に比べると穏やかなため、反応を触媒するためには基質を多点で活性化することがしばしば必要です。これは触媒が基質と多点で相互作用をつくりやすいことにつながります。私たちは有機触媒ならではの多点相互作用に基づく分子認識を利用して、生体酵素でも実現できなかった不斉合成反応を開発してきました。
分子内ヘテロマイケル付加反応
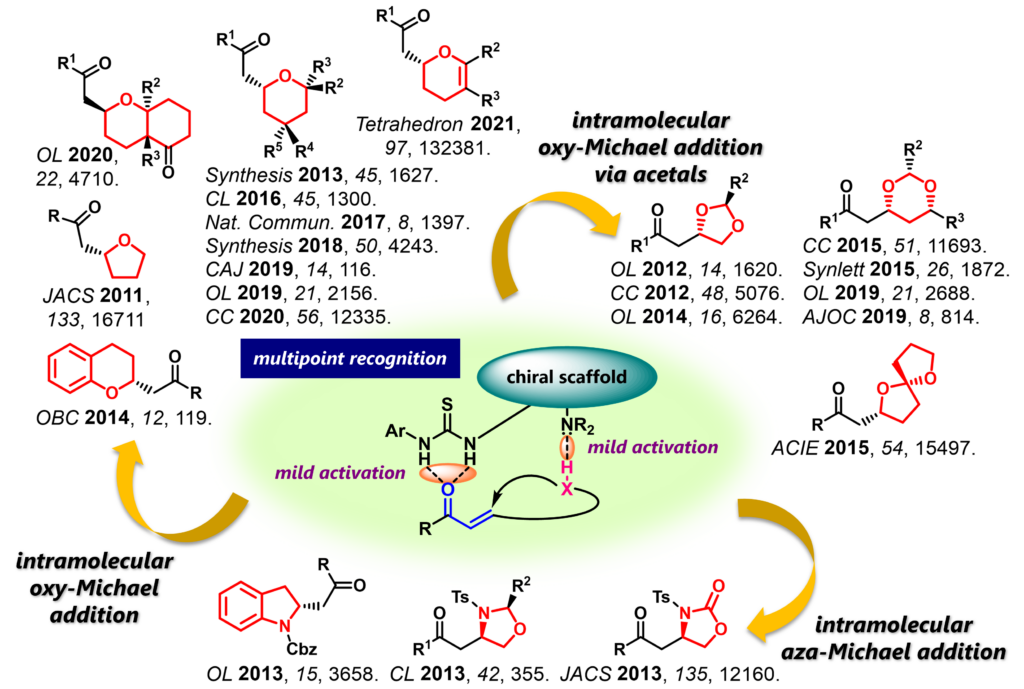
分子内ヘテロマイケル付加反応は生物活性が期待される複素環を簡便に合成できる反応です。しかし分子内反応は非常に速いため、エナンチオ選択性を得ることが難しい反応でした。そこで私たちは穏やかな酸と塩基を同一分子内に持つ有機触媒(アミノチオ尿素、リン酸など)に焦点を当てました。これらの触媒は水素結合を多点でつくりながら基質を活性化し、効果的なキラル環境を構築します。私たちはこの手法により様々な複素環化合物の不斉合成を達成しました。
- Asano, K.; Matsubara, S. J. Am. Chem. Soc. 2011, 133, 16711–16713.
- Asano, K.; Matsubara, S. Org. Lett. 2012, 14, 1620–1623.
- Okamura, T.; Asano, K.; Matsubara, S. Chem. Commun. 2012, 48, 5076–5078.
- Fukata, Y.; Asano, K.; Matsubara, S. Chem. Lett. 2013, 42, 355–357.
- Fukata, Y.; Miyaji, R.; Okamura, T.; Asano, K.; Matsubara, S. Synthesis 2013, 45, 1627–1634.
- Miyaji, R.; Asano, K.; Matsubara, S. Org. Lett. 2013, 15, 3658–3661.
- Fukata, Y.; Asano, K.; Matsubara, S. J. Am. Chem. Soc. 2013, 135, 12160–12163.
- Miyaji, R.; Asano, K.; Matsubara, S. Org. Biomol. Chem. 2014, 12, 119–122.
- Yoneda, N.; Hotta, A.; Asano, K.; Matsubara, S. Org. Lett. 2014, 16, 6264–6266.
- Matsumoto, A.; Asano, K.; Matsubara, S. Chem. Commun. 2015, 51, 11693–11696.
- Matsumoto, A.; Asano, K.; Matsubara, S. Synlett 2015, 26, 1872–1874.
- Yoneda, N.; Fukata, Y.; Asano, K.; Matsubara, S. Angew. Chem., Int. Ed. 2015, 54, 15497–15500.
- Yoneda, N.; Matsumoto, A.; Asano, K.; Matsubara, S. Chem. Lett. 2016, 45, 1300–1303.
- Yoneda, N.; Fujii, Y.; Matsumoto, A.; Asano, K.; Matsubara, S. Nat. Commun. 2017, 8, 1397.
- Asano, K.; Matsubara, S. Synthesis 2018, 50, 4243–4253.
- Matsumoto, A.; Asano, K.; Matsubara, S. Chem.—Asian J. 2019, 14, 116–120.
- Kurimoto, Y.; Nasu, T.; Fujii, Y.; Asano, K.; Matsubara, S. Org. Lett. 2019, 21, 2156–2160.
- Matsumoto, A.; Asano, K.; Matsubara, S. Org. Lett. 2019, 21, 2688–2692.
- Matsumoto, A.; Asano, K.; Matsubara, S. Asian J. Org. Chem. 2019, 8, 814–818.
- Wada, Y.; Murata, R.; Fujii, Y.; Asano, K.; Matsubara, S. Org. Lett. 2020, 22, 4710–4715.
- Murata, R.; Matsumoto, A.; Asano, K.; Matsubara, S. Chem. Commun. 2020, 56, 12335–12338.
- Murata, R.; Asano, K.; Matsubara, S. Tetrahedron 2021, 97, 132381.
官能基が集積した四置換不斉炭素の構築
創薬では二次元的な分子よりもsp3炭素を豊富に含む三次元的な分子が高いヒット確率を示し、中でも四置換炭素を持つ分子は効果的です。さらにその4つの置換基に官能基を豊富に持つキラル分子は魅力的です。穏やかな有機触媒は立体選択性だけではなく化学選択性にも長けています。すなわち様々な官能基を持つ基質でも特定の官能基を選んで反応させることができます。私たちはこの特徴を活かして、複素環や様々な官能基を集積した四置換不斉炭素を構築する反応を開発しています。
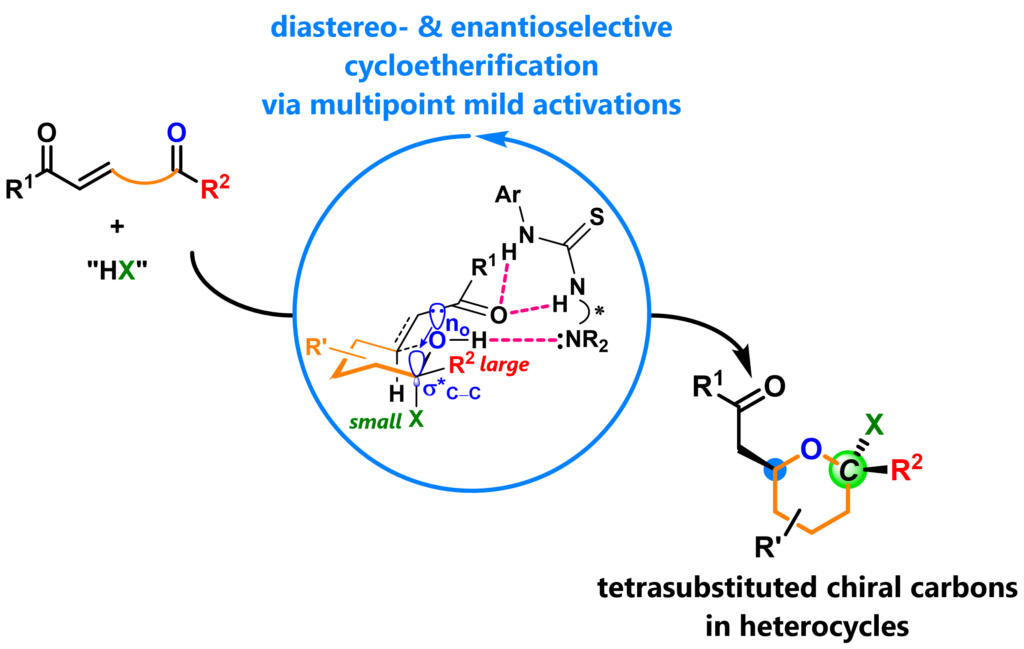
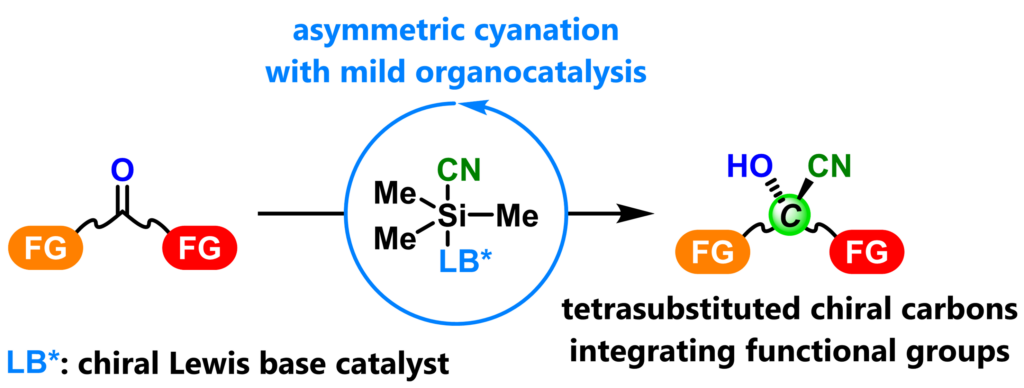
- Yoneda, N.; Fukata, Y.; Asano, K.; Matsubara, S. Angew. Chem., Int. Ed. 2015, 54, 15497–15500.
- Yoneda, N.; Matsumoto, A.; Asano, K.; Matsubara, S. Chem. Lett. 2016, 45, 1300–1303.
- Yoneda, N.; Fujii, Y.; Matsumoto, A.; Asano, K.; Matsubara, S. Nat. Commun. 2017, 8, 1397.
- Asano, K.; Matsubara, S. Synthesis 2018, 50, 4243–4253.
- Matsumoto, A.; Asano, K.; Matsubara, S. Chem.—Asian J. 2019, 14, 116–120.
- Kurimoto, Y.; Nasu, T.; Fujii, Y.; Asano, K.; Matsubara, S. Org. Lett. 2019, 21, 2156–2160.
- Wada, Y.; Murata, R.; Fujii, Y.; Asano, K.; Matsubara, S. Org. Lett. 2020, 22, 4710–4715.
- Murata, R.; Matsumoto, A.; Asano, K.; Matsubara, S. Chem. Commun. 2020, 56, 12335–12338.
- Nagano, T.; Matsumoto, A.; Yoshizaki, R.; Asano, K.; Matsubara, S. Commun. Chem. 2022, 5, 45.
軸不斉化合物の合成

二官能性有機触媒により分子の形を認識する手法を利用して、有機分子の軸不斉を制御する反応を開発しました。これにより、医農薬、光電材料、触媒などに利用が期待できる軸不斉化合物の高エナンチオ選択的合成を実現し、学術的にも二官能性有機触媒の新しい不斉制御機構を開拓しました。
- Miyaji, R.; Asano, K.; Matsubara, S. J. Am. Chem. Soc. 2015, 137, 6766–6769.
- Miyaji, R.; Asano, K.; Matsubara, S. Chem.—Eur. J. 2017, 23, 9996–10000.
- Miyaji, R.; Wada, Y.; Matsumoto, A.; Asano, K.; Matsubara, S. Beilstein J. Org. Chem. 2017, 13, 1518–1523.
- Wada, Y.; Matsumoto, A.; Asano, K.; Matsubara, S. RSC Adv. 2019, 9, 31654–31658.
α,β-不飽和アシルアンモニウム触媒
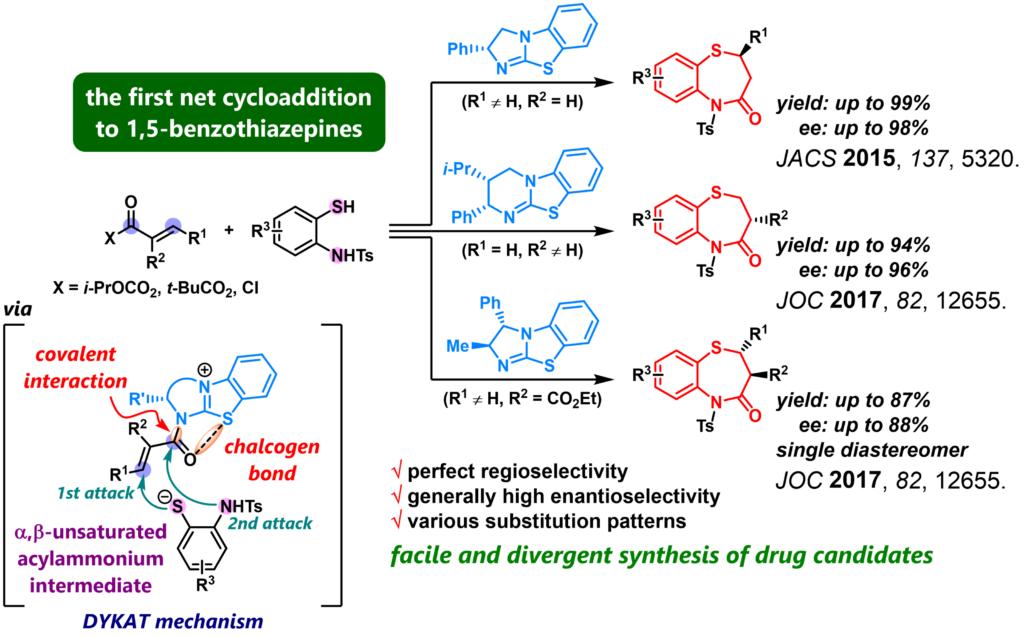
共有結合とカルコゲン結合を利用した多点活性化触媒(α,β-不飽和アシルアンモニウム種を鍵中間体とする触媒)により、硫黄のマイケル付加を経る不斉環化反応を開発しました。特に、代表的な医薬候補分子である1,5-ベンゾチアゼピン類の高位置・立体選択的環化付加合成法を開発し、その簡便・迅速な不斉ライブラリ合成を可能にしました。また、抗うつ剤・チアゼシムの短工程合成も実現しました。
